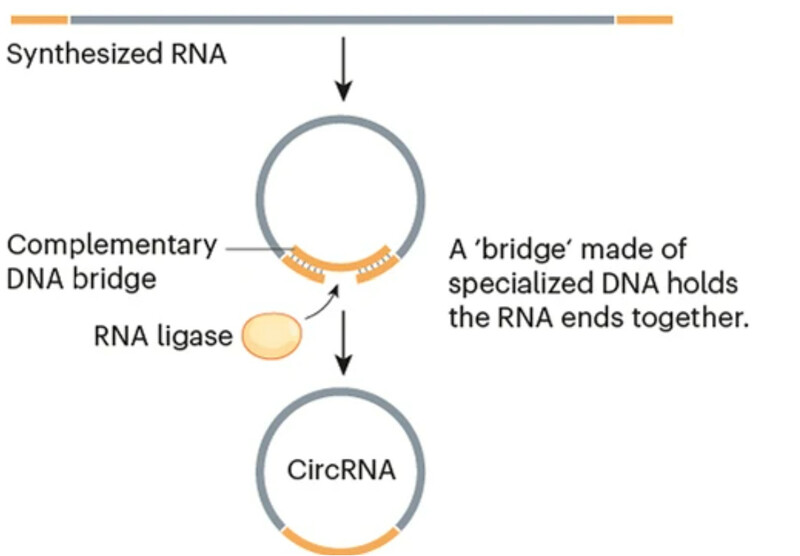
알엔에이(RNA)는 선형분자로 세포에 들어오면 양 끝에서 공격받아 쉽게 파괴된다는 단점이 있다.(위) 과학자들은 알엔에이 말단 염기서열에 상보적인 디엔에이(DNA) 조각을 넣어 양 끝을 이어붙이는 방법으로 원형알엔에이를 만들어 안정성을 크게 높였다.(아래) ‘네이처’ 제공
| 강석기 과학칼럼니스트
닭이 먼저냐 달걀이 먼저냐.
분야마다 두 사건의 선후 관계가 애매한 문제가 있기 마련이고 생명과학도 예외가 아니다. 바로 ‘디엔에이(DNA)가 먼저냐 단백질이 먼저냐’라는 질문이 대표적이다. 디엔에이는 단백질을 이루는 아미노산의 정보를 지니므로 먼저일 것 같지만 화학반응을 촉매하는 효소인 단백질이 있어야 디엔에이를 만들 수 있으니 그렇지도 않다.
1970년대 말 놀라운 발견이 이 논쟁을 끝냈다. 디엔에이와 비슷한 분자인 알엔에이(RNA)가 유전정보 저장과 함께 효소로도 작용할 수 있다는 사실이 밝혀진 것이다. 1986년 미국 분자생물학자 월터 길버트는 생명의 기원을 설명하며 자신의 염기서열을 스스로 복제하는 알엔에이 분자가 최초의 생명체였다는 ‘알엔에이 세계’ 가설을 내놓았다. 약 40억년 전 지구에서 알엔에이로 이뤄진 생명체가 먼저 나타났고 그 뒤 좀 더 안정한 분자인 디엔에이가 정보 저장을 맡고 촉매 효율이 더 높은 단백질이 효소를 맡게 진화했다는 시나리오다.
이런 심오함에도 알엔에이 세계는 물론 알엔에이도 대중매체에 거의 등장하지 않았다. 그런데 2020년 코로나19가 창궐하면서 엠알엔에이(mRNA)라는 용어가 이제 디엔에이만큼이나 익숙해졌다. 참고로 엠알엔에이는 디엔에이 유전자의 정보를 단백질로 번역하는 과정을 매개하는 알엔에이로 m은 ‘전령’을 뜻한다. 항원인 바이러스 단백질 대신 그 정보를 지닌 엠알엔에이를 넣어 사람 세포가 바이러스 단백질을 만들게 한 것이다. 물고기가 아니라 물고기를 낚는 법을 알려주는 셈이다.
지난주 노벨상 주간에 발표된 과학상 가운데 엠알엔에이 백신 개발자들이 받은 생리의학상이 언론의 관심을 가장 많이 받았다. 빠르면 2021년에도 받을 것이라는 예상이 있었는데 오히려 늦은 셈이다. 아무튼 필자를 포함해 우리나라 사람 대다수가 엠알엔에이 백신을 접종받았으니 수상자들에게 감사의 마음을 전한다.
코로나 백신 성공을 계기로 엠알엔에이 의약품을 개발하는 연구가 붐을 이루면서 최신 기술이 속속 나오고 있다. 지난달 학술지 ‘네이처’에는 엠알엔에이 염기서열을 최적화해 안정성과 단백질 합성 효율을 높이는 기법을 소개한 논문이 실렸다. 엠알엔에이의 단점은 불안정성으로 세포에 투입된 뒤 얼마 못 가 파괴된다는 점이다. 그런데 단백질 정보를 온전히 지니면서도 좀 더 안정한 염기서열을 찾는 방법이 개발돼 기존보다 적은 양의 엠알엔에이가 들어 있고 상온에서도 유통과 보관이 가능한 백신이 나올 길이 열렸다.
지난주 ‘네이처’에는 원형알엔에이라는 새로운 구조가 개발돼 알엔에이 의약품의 안정성과 효율을 획기적으로 높일 것이라는 기사가 실렸다. 기존 알엔에이는 선형분자라 양 끝에서부터 쉽게 파괴되는데 양 끝을 이어 붙여 원형으로 만들면 오래 살아남는다. 이런 안정성 덕분에 원형알엔에이 자체가 표적을 인식해 작용하는 약물로 작용할 수 있다. 중국 연구진은 엠알엔에이를 원형으로 만든 백신을 개발해 지난 8월 임상시험에 들어갔다.
현재 세계 각국의 거대 제약회사는 물론 많은 스타트업이 각자의 아이디어로 다양한 알엔에이 의약품을 만드는 연구에 뛰어들었다. 국내 한 업체도 최근 원형알엔에이를 깔끔하게 만들어 잠재적인 부작용을 최소화하는 방법을 개발했다는 논문을 발표했다. 40억년 전 디엔에이와 단백질에 주도권을 내주고 뒤에 물러나 있던 알엔에이가 다시 전면에 나서고 있다.